Minha senha
Por favor digite seu email cadastrado em nosso sistema que enviaremos uma nova senha de acesso.
Atualizado em 16/05/2023
INTRODUÇÃO
O tratamento padrão para câncer de mama inicial é a cirurgia conservadora e biópsia de linfonodo sentinela, cujo acompanhamento a posteriori pode resultar em aproximadamente 14,3% a 20% de recorrências locais que necessitam de reoperação. Diretrizes do National Comprehensive Cancer Network sugerem que, para pacientes com recorrência local após setorectomia e BLS, repetir BLS (rBLS) pode ser uma opção. Porém, preocupações existem de que a cirurgia inicial da mama ou axila podem alterar parcialmente o fluxo linfático, dificultando o reconhecimento do linfonodo sentinela. Port et al. relataram que dissecção parcial prévia ou biópsia de linfonodo não afetaram a taxa de sucesso de rSLNB. No entanto, ainda existe controvérsia sobre se o rBLS é seguro e eficiente. Para avaliar a necessidade e a sobrevida a longo prazo de rBLS para estadiamento axilar entre pacientes com recidiva local, foi desenvolvido o presente estudo.
MÉTODO
O trial foi conduzido a partir de uma coorte utilizando o banco de dados norte-americano SEER entre 2000 e 2017, com pacientes apresentando recidiva local e axila negativa clinicamente. O tipo de cirurgia axilar foi dividido em: sem cirurgia axilar (0 linfonodos analisados), rBLS (1 a 5 linfonodos analisados) e EA (maior ou igual a 6 linfonodos axilares). O desfecho primário foi definido como o tempo de sobrevida desde o diagnóstico de recidiva até a data da morte por qualquer causa. O desfecho secundário foi a sobrevida geral entre as coortes sem cirurgia e com cirurgia axilar. O principal objeto do estudo foi a comparação da sobrevida entre os grupos rBLS e EA.
RESULTADOS
No período definido, foram selecionados 2141 pacientes, sendo que 524 não receberam cirurgia axilar (24,47%) e 1617 receberam cirurgia axilar (75,53%) - 1268 rBLS e 349 EA.
Em comparação com as pacientes sem cirurgia, as pacientes com cirurgia axilar eram mais jovens (com idade superior a 65 anos: 46,2% vs 56,1%, p < 0,001), tiveram recidiva mais precoce (18,1% vs 8,8% para diagnóstico dentro de 2 anos, p < 0,001), fizeram mais mastectomia (73,5% vs 56,9%, p < 0,001), fizeram mais radioterapia (14,9% vs 10,3%, p = 0,008) e fizeram mais quimioterapia (25,7% vs 19,3%, p = 0,003).
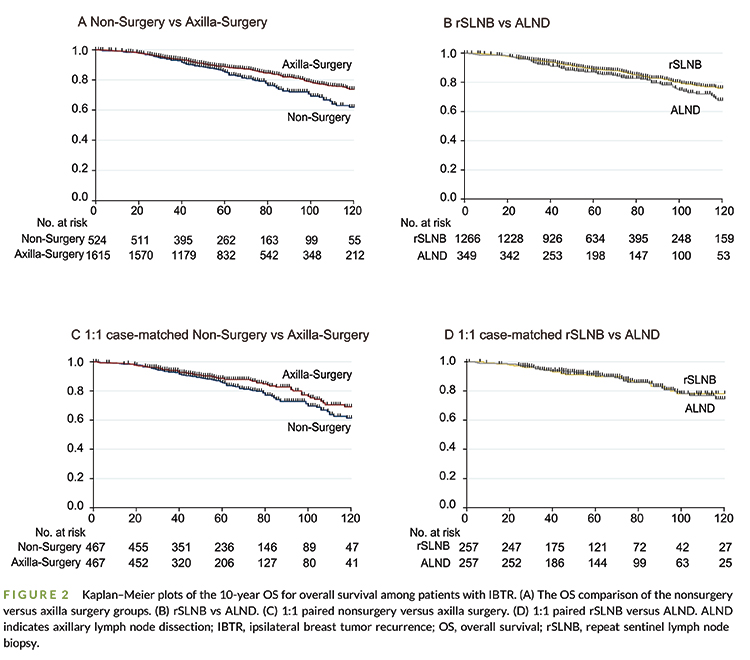
Os pacientes do grupo sem cirurgia tiveram uma SG pior em 10 anos do que aqueles no grupo de cirurgia da axila (61,9% vs 73,8%; p = 0,001). Não houve diferença significativa na SG de 10 anos entre os grupos rBLS e EA (78,2% vs 74,5%, p = 0,927).
A análise de sobrevida das coortes pareadas 1:1 mostrou que o grupo de cirurgia da axila apresentou melhores resultados de sobrevida especifica para câncer de mama (SECM) (93,7% vs 85,1%; p = 0,037), e os grupos rBLS e EA tiveram resultados semelhantes (92,1% vs 87,8%, p = 0,261).
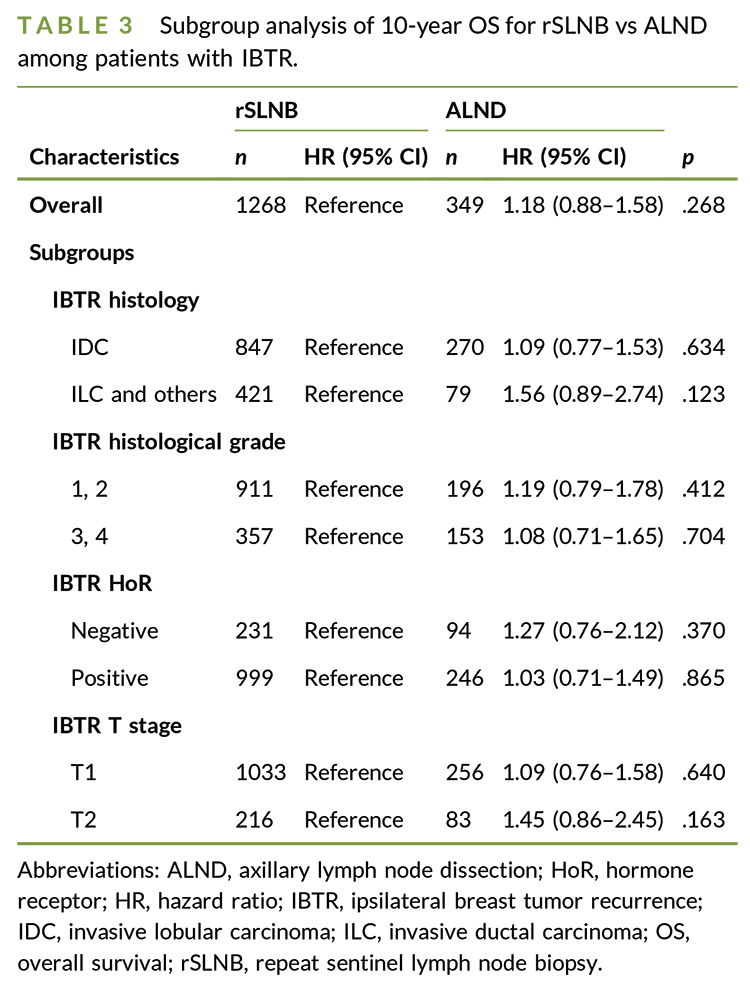
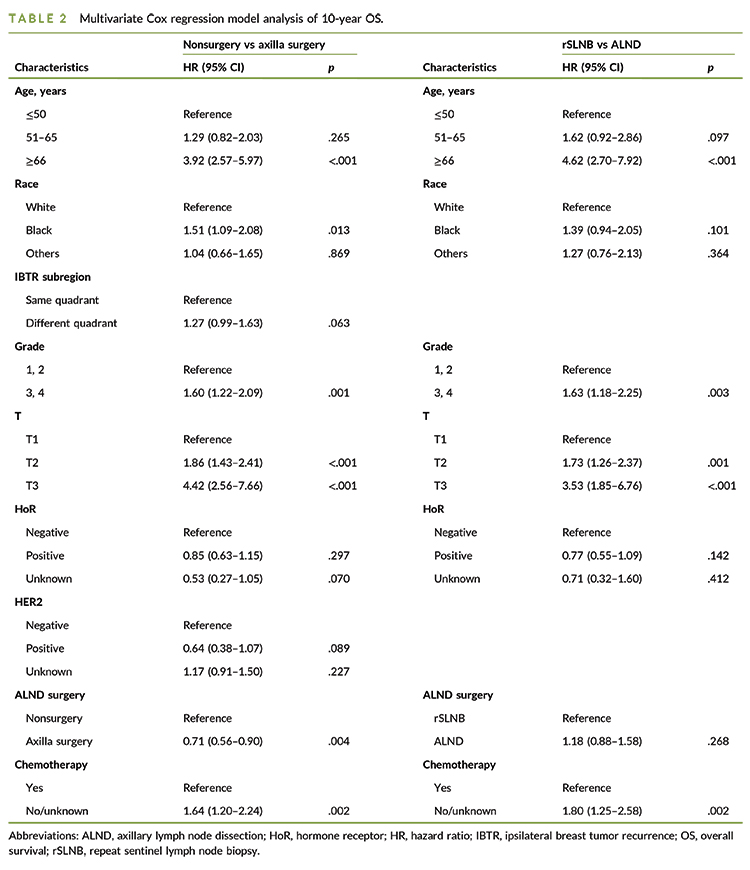
O tratamento com cirurgia axilar foi confirmado como um fator favorável independente sobre o grupo sem cirurgia em relação a SG de 10 anos (HR, 0,71; IC de 95%, 0,56–0,90; p = 0,004) e SECM de 10 anos (HR, 0,68; IC 95%, 0,47–0,98; p = 0,041). O grupo de rBLS não apresentou significância estatística para benefício de sobrevida sobre EA, independentemente de SG ou SECM (SG HR de 10 anos, 1,18; IC de 95%, 0,88‐1,58; p = 0,268; SECM HR, 1,27; IC 95%, 0,82–1,97; p = 0,278).
O presente estudo então sugeriu que realizar o estadiamento axilar cirúrgico foi associado a menor mortalidade geral, enquanto a escolha de EA ou rBLS não afetou a sobrevida de 10 anos. Assim, o rBLS pode ser considerado para cirurgia axilar entre as pacientes com recidivas locais. Um viés de seleção deve ser considerado porque pacientes com tumores recorrentes menores e com melhores graus histológicos eram propensos a rBLS. Foi realizado análise de coorte pareada 1:1 e análise de Cox multivariável. Ambos os métodos verificaram os resultados de que o rBLS teve um benefício de sobrevida semelhante ao EA.
Outro fator a ser considerado são as falhas de BLS e rBLS que não foram analisadas, devido não constar essa informação no SEER. Adicional a isso, o intervalo mínimo necessário entre a primeira e a repetição do BLS e o tempo de restabelecimento da drenagem linfática ainda não foi estabelecido. Portanto, mais estudos prospectivos são necessários para se validar a segurança e a precisão do rBLS.

Membro da Comissão de Educação Continuada da SBM - Regional SP