Minha senha
Por favor digite seu email cadastrado em nosso sistema que enviaremos uma nova senha de acesso.
Atualizado em 20/12/2021
INTRODUÇÃO
O gene HER-2 superexpresso está presente em 10-20% dos tumores de mama estadios iniciais, e está associado com maior agressividade e aumento no risco de recorrência da doença.
Trastuzumabe é um anticorpo monoclonal, humanizado IgG1, que se liga ao domínio extracelular da proteína HER-2. No cenário de doença HER-2 metastática, seu uso associado à quimioterapia tem impacto no aumento do tempo livre de progressão de doença e na sobrevida global. Benefícios do uso da medicação também foram vistos no cenário não-metastático, e hoje trastuzumabe combinado com quimioterapia é considerado terapia padrão tanto para pacientes metastáticas quanto estadios iniciais do carcinoma de mama HER-2 positivo.
Entretanto, não está claro se o nível de amplificação do HER2, características tumorais, em particular o status do receptor de estrógeno (RE), ou fatores de risco associados ao paciente teriam influência na magnitude do benefício e duração do tratamento.
DETALHES DO ESTUDO
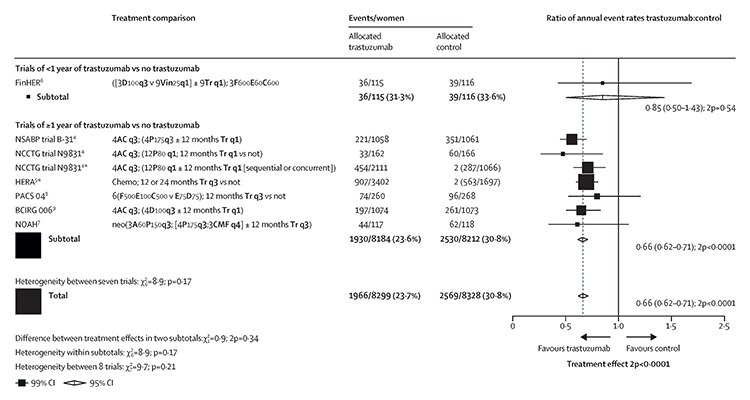
Foi realizada uma metanálise, pelo The Early Breast Cancer Trialists´ Collaborative Group (EBCTCG), que incluiu 7 estudos controlados e randomizados que compararam o uso de quimioterapia e trastuzumabe com apenas quimioterapia em pacientes com tumores HER2 positivo e estadios iniciais.
O objetivo da metanálise foi avaliar os benefícios a longo prazo e os riscos associados ao uso do trastuzumabe em relação à sobrevida livre de doença e mortalidade, e avaliar também se as características dos tumores e das pacientes afetavam os resultados.
RESULTADOS
A coorte analisada incluiu 13.864 mulheres com tumores estadio inicial e HER2 positivo, que foram randomizadas entre fevereiro de 2000 e dezembro de 2005, para receberam quimioterapia + trastuzumabe ou apenas quimioterapia.
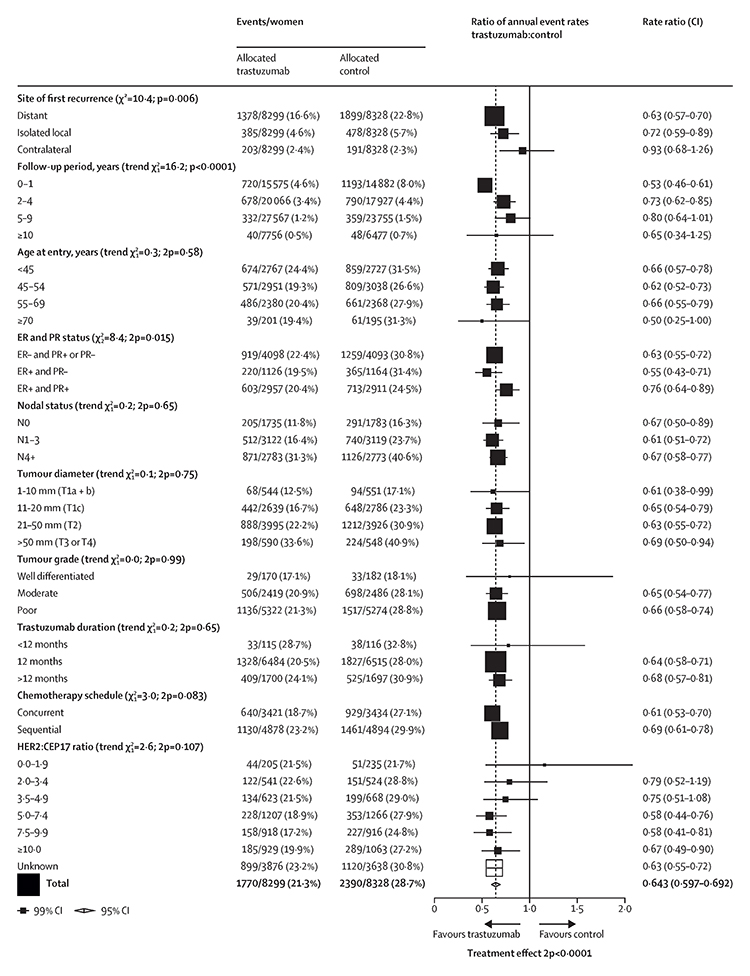
Como critério de inclusão nos trials, as pacientes deveriam ter axila positiva ou axila negativa e serem de alto risco (definido genericamente como tumores grau 3, >1cm se RE negativo ou >2cm se RE positivo).
A grande maioria das pacientes (56.1%) foi submetida a esquema sequencial de 12 semanas de antracíclicos, seguido de 12 semanas de taxanos (estudos NSABP B-31, NCCTG N9831 e BCIRG 006). Em todos os trials, a endocrinoterapia foi recomendada para tumores com receptor hormonal positivo.
A duração do tratamento foi de 12 meses em todos os trials, exceto o estudo FinHER, que testou o trastuzumabe por 9 semanas, e o estudo HERA que incluiu um subgrupo de tratamento com 24 meses.
A média de follow-up foi de 10.7 anos e dessas mulheres 3.685 (26,6%) apresentaram recidiva.
Na análise combinada dos trials, foi observada uma redução bastante significativa em recorrência (RR 0.66, p<0.0001) e na mortalidade (0.67, p<0.0001) em favor da quimioterapia associada ao trastuzumabe.
No grupo trastuzumabe foi observada redução absoluta em 10 anos para recorrência de 9% (p<0.0001), sendo 6.4% (p<0.0001) para mortalidade específica por câncer e de 6,5% (p<0.0001) para mortalidade por qualquer causa. Não houve, nesse mesmo grupo, aumento em mortalidade sem recorrência de câncer (RR 0.90, p=0.35), mortalidade por eventos cardiovasculares (1.23, p=0.44) ou mortalidade por cânceres em outros sítios além da mama (0.79, p=0.24).
Foi observado também redução em recorrência local (RR 0.72), recorrência à distância (0.63), mas não em incidência de câncer contralateral e de metástase cerebral como primeiro sítio de metástase no grupo trastuzumabe.
A maior redução proporcional em recorrência, observada no grupo trastuzumabe, durante o follow-up ocorreu nos anos 0-1 (RR 0.53), com menor impacto nos anos 2-4 (RR 0.73) e nos anos 5-9 (0.80).
Em relação ao subgrupos RE positivo e RE negativo, houve redução proporcional de recorrência muito similar (RR 0.67 versus 0.62, respectivamente), variando apenas no momento da recorrência, mais precoce nos tumores RE negativo e mais tardios nos RE positivos. A média na redução absoluta da mortalidade em 10 anos para RE negativo foi de 6.9% e RE positivo 5.1%.
Não foi observada diferença em relação à redução de recorrência entre a administração do trastuzumabe concomitantemente à quimioterapia ou sequencial à mesma.
DISCUSSÃO
Essa metanálise corrobora com os dados de que, para pacientes com tumores de mama HER2 positivo iniciais, a adição de trastuzumabe à quimioterapia reduz significativamente a recorrência e mortalidade por câncer de mama, durante a primeira década de follow-up em aproximadamente um terço.
Para a população analisada, isso se traduziu em média numa redução absoluta em 10 anos de 9% para recorrência e 6,4% em mortalidade por câncer de mama, comparado com apenas quimioterapia.
O maior benefício foi observado em relação a diminuição da recorrência à distância, embora também tenha sido observado diminuição da recorrência local; o mesmo não foi visto para recorrência contralateral.
A análise de subgrupos em relação a características patológicas tumoral, foi observada redução proporcional similar, independente do status nodal, grau tumoral, diâmetro do tumor e subtipo histológico. Embora a redução proporcional tenha sido similar entre subgrupos de axila positiva ou negativa, a redução absoluta do risco em 5 anos foi maior quanto pior o comprometimento linfonodal dessas pacientes, pelo maior risco de recorrência absoluto por elas apresentado.
A redução proporcional em recorrência não variou em relação à idade, IMC, duração do tratamento com trastuzumabe, fatores histopatológicos tumoral (incluindo tamanho do tumor, status nodal, grau tumoral, subtipo histológico), embora na coorte avaliada quase não houvesse mulheres acima de 70 anos, ou com tumores baixo grau ou lobulares.
CONCLUSÃO
O uso do trastuzumabe durante 1 ano, associado à quimioterapia, no cenário adjuvante para pacientes com tumores HER-2 positivo em estadios iniciais, reduz a recorrência e a mortalidade por câncer de mama em um terço, benefício esse observado independente das características do tumor ou da paciente.
REFERÊNCIA
Early Breast Cancer Trialists’ Collaborative group (EBCTCG). Trastuzumab for early-stage, HER2-positive breast cancer: a meta-analysis of 13 864 women in seven randomised trials. Lancet Oncol. 2021 Aug;22(8):1139-1150. doi: 10.1016/S1470-2045(21)00288-6. PMID: 34339645; PMCID: PMC8324484.

Residente do 2° ano de Mastologia do Hospital Sírio Libanês (2020-2022) Ginecologista e Obstetra pelo Hospital Universitário de Maringá-PR.