Tipo de terapia endócrina adjuvante e sobrevida livre de doença em pacientes com câncer de mama RH positivo/HER2-positivo precoce: análise do estudo ShortHer randomizado de fase III



INTRODUÇÃO
Os tumores de mama HER-2 positivos são muito heterogêneos, o que implica em situações clínicas, resultados e sensibilidade do tratamento muito diferentes. Por exemplo, pacientes RH positivo/HER2-positivo apresentam um menor risco de recaída nos primeiros 3 a 5 anos após o diagnóstico em comparação com pacientes com RH-negativo/HER2-positivo. A hormonioterapia ideal para pacientes com RH-positivo/HER2-positivo ainda não está claramente elucidada. O EBCTCG (2015) estabeleceu os inibidores de aromatase como o tratamento preferencial para pacientes pós-menopausa com uma redução significativa no risco de recaída de cerca de 30% em relação ao tamoxifeno. Este efeito foi mantido inalterado em ambos os subgrupos HER2-positivos e HER2-negativos. No entanto, o status HER2 não estava disponível para 70% dos pacientes nesta metanálise e o subgrupo HER2-positivo foi limitado no tamanho da amostra. Em pacientes pré menopausa com RH-positivo submetidas à supressão da função ovariana, o inibidor de aromatase é superior ao tamoxifeno, conforme demonstrado pelos ensaios TEXT e SOFT, com um ganho de sobrevida livre de doença distante em 8 anos de 4%. No entanto, os pacientes HER2-negativos obtiveram benefício do inibidor de aromatase (5,4% de benefício absoluto em DFS em 8 anos, HR 0,70), enquanto o tamoxifeno foi numericamente superior no subgrupo HER2-positivo (n = 695, 3,2% de diferença em DFS em 8 anos). Uma limitação importante de todos esses estudos é a pequena proporção de pacientes RH-positivos/HER2-positivos que receberam terapia anti-HER2 como parte do tratamento sistêmico. Portanto, é necessário avaliar a opção ideal de terapia endócrina para esses pacientes no contexto do tratamento adjuvante padrão.
MÉTODOS
Nesse estudo foram analisados pacientes com tumores RH-positivo e HER2-positivo constantes do estudo ShortHER (NCT00629278) que compara trastuzumabe de 1 ano versus 9 semanas adicionado à quimioterapia. A hormonoterapia adjuvante seguiu os padrões locais de acordo com as diretrizes.
Identificados 853 pacientes com tumores iniciais RH-positivo/HER2-positivo, mais da metade dos pacientes (59,6%) receberam AI, 23,8% receberam TAM e 16,6% TAM-AI. Não houve diferenças significativas no tipo de hormonioterapia adjuvante de acordo com o estágio da doença, grau histológico e braço de randomização.
RESULTADOS
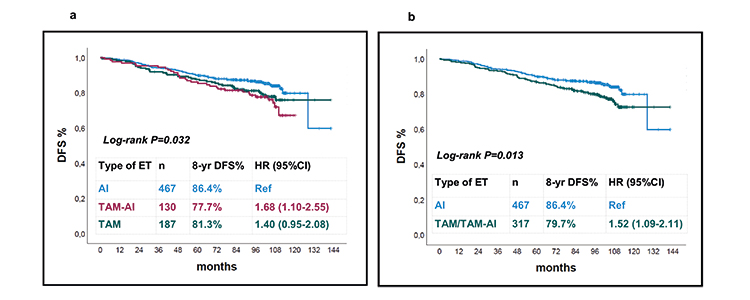
Em um acompanhamento médio de 8,7 anos, as taxas de DFS foram: 86,4% para AI, 81,3% para TAM e 77,7% para TAM-AI (p = 0,032). Análises univariadas de cox-regressão com o grupo AI como referência mostraram um HR de 1,40 (95% CI 0,95–2,08, p = 0,089) para TAM e um HR de 1,68 (95% CI 1,10–2,55, p = 0,016) para TAM -AI. Uma vez que o grupo AI surgiu como aquele com o prognóstico mais favorável e os pacientes tratados com TAM ou TAM-AI mostraram resultados semelhantes, eles compararam DFS para pacientes tratados com AI versus pacientes tratados com TAM ou TAM-AI. As taxas de DFS em 8 anos foram de 86,4% para AI e 79,7% para TAM/TAM-AI, com uma diferença absoluta de 6,7% (p = 0,013). Em termos de OS, não houve diferença entre a hormonioterapia recebida.
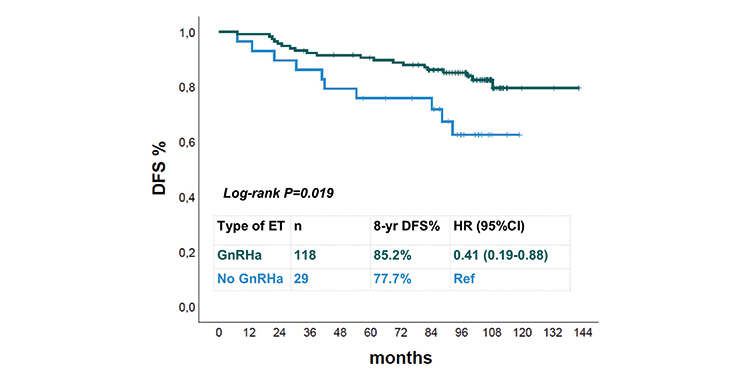
Em análise das pacientes na pré-menopausa com idade ≤45 anos (n = 147) que utilizaram GnRH, 97% receberam TAM ou TAM-AI e apenas quatro pacientes receberam AI. Trinta pacientes neste grupo experimentaram um evento DFS. O GnRHa foi associado a taxas de DFS em 8 anos de 85,2 vs 62,6% (HR 0,41, IC 95% 0,19–0,88, p = 0,023).
Nos estudos TEXT e SOFT, para pacientes submetidos a OFS, o TAM foi numericamente superior ao AI no subgrupo de pacientes HER2-positivos. A metanálise EBCTCG comparando AI vs TAM no contexto de OFS para pacientes na pré-menopausa também sugeriu maior benefício de AI vs TAM na doença HER2-negativa do que na doença HER2-positiva (RR 0·65 vs 1·08, p=0·021). No entanto, o subgrupo HER2-positivo foi limitado em tamanho de amostra com um pequeno número de eventos. Além disso, a diferença entre tumores HER2-positivos e HER2-negativos não alcançaram significância estatística.
Um ponto chave final desse estudo é a análise exploratória do papel da OFS para pacientes na pré-menopausa. A adição de GnRHa a hormonioterapia (principalmente TAM ou TAM-AI) para pacientes na pré-menopausa com idade ≤45 anos foi associada a um DFS significativamente melhor. As análises de subgrupo do estudo SOFT demonstraram melhores resultados para OFS adicionado ao TAM na doença HER2-positiva.
Uma das limitações do estudo, impostas pelos autores, foi a não possibilidade de se avaliar adequadamente a duração da terapia além de 5 anos e a adesão/interrupções do tratamento. Além disso, as pacientes na perimenopausa não foram claramente definidas e outros meios de OFS além do GnRHa não foram capturados após a triagem. Todos os pacientes receberam trastuzumabe, embora metade deles tenha recebido tratamento de 9 semanas, o que não é o padrão atual. Finalmente, uma grande proporção de pacientes incluídos no estudo ShortHER seriam hoje tratadas com uma abordagem neoadjuvante seguida de trastuzumabe-emtansina em caso de não resposta patológica completa, portanto, a transferibilidade dos dados para pacientes contemporâneos do mundo real pode não ser direto.
CONCLUSÃO
Em conclusão, os achados apoiam o uso de IA como terapia adjuvante para pacientes HR-positivos/ HER2-positivos no contexto do tratamento adjuvante, associado com quimioterapia e trastuzumabe. Em pacientes na pré-menopausa, o uso de OFS prolonga o DFS. No entanto, a terapia endócrina oral ideal (AI ou TAM) neste subgrupo permanece incerta e justifica uma avaliação mais aprofundada em grandes coortes de pacientes tratados com terapia adjuvante padrão.

Paulo Gustavo Tenório do Amaral
Médico Mastologista pela FMUSP/SP
Leituras recomendadas