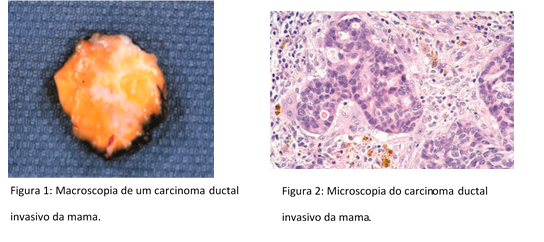
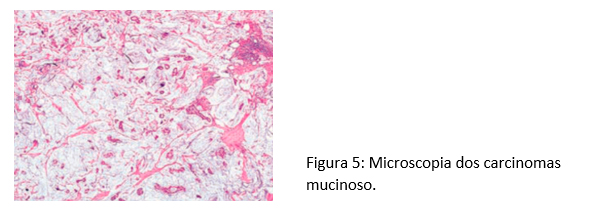
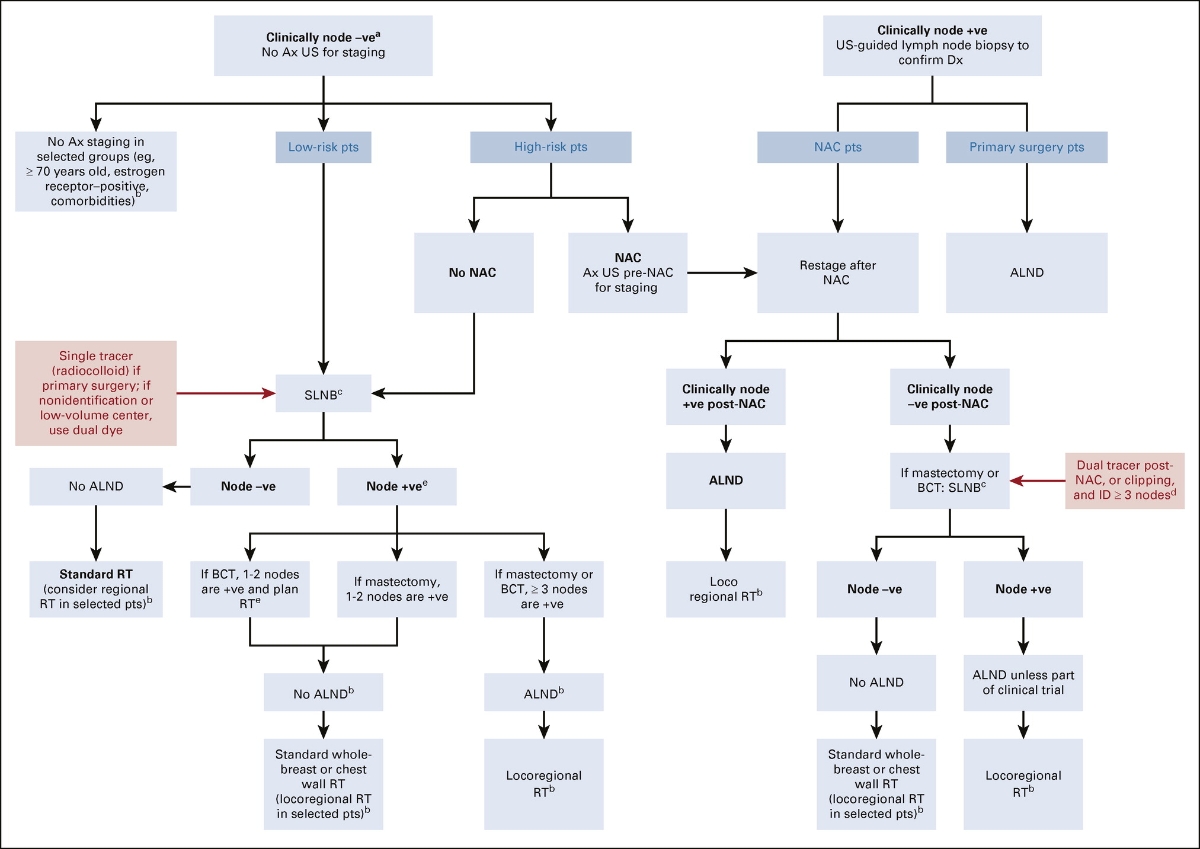
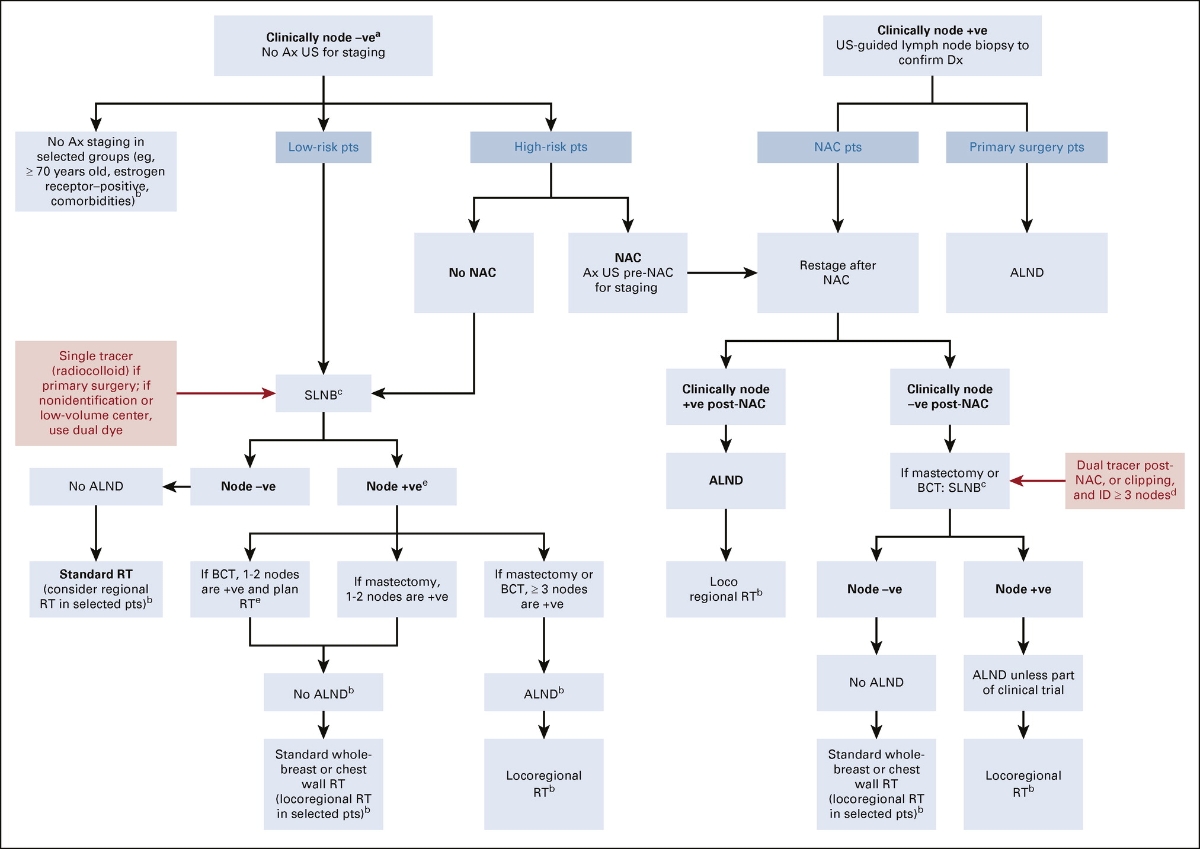
Diagnóstico por Imagem – Rastreamento
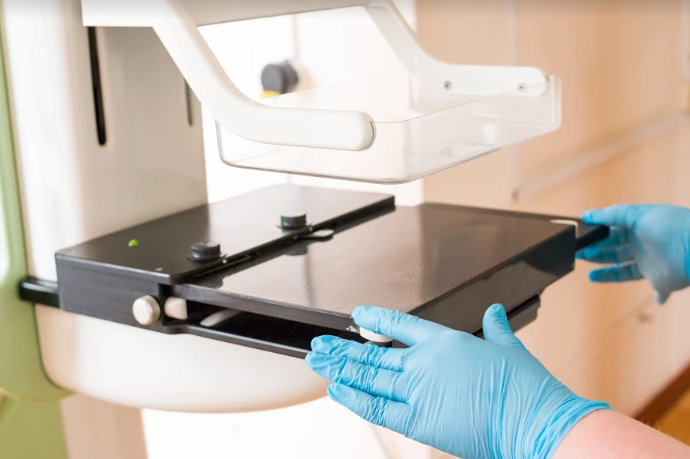
O rastreamento do câncer de mama deve ser realizado com mamografia a partir dos 40 anos, anualmente, conforme recomendação das sociedades americanas como o Colégio Americano de Radiologia (ACR), Colégio Americano de Cirurgiões e Sociedade Americana do Câncer e das sociedades brasileiras como a Sociedade Brasileira de Mastologia, Colégio Brasileiro de Radiologia e FEBRASGO. O rastreamento mamográfico pode reduzir em 30% ou mais a mortalidade por câncer de mama.
Uma particularidade do câncer de mama no Brasil e em outros países em desenvolvimento é que a sua incidência nas mulheres com idade entre 40 e 50 anos é proporcionalmente maior que a de países desenvolvidos.
Em 2012, o Colégio Brasileiro de Radiologia e Diagnóstico por Imagem (CBR), a Sociedade Brasileira de Mastologia (SBM) e a Federação Brasileira das Associações de Ginecologia e Obstetrícia (Febrasgo), por meio da Comissão Nacional de Mamografia, publicaram as recomendações para o rastreamento por imagem do câncer de mama no Brasil.
RECOMENDAÇÕES PARA O RASTREAMENTO
RASTREAMENTO DAS MULHERES COM RISCO POPULACIONAL USUAL
Mamografia
- Rastreamento anual para mulheres entre 40 a 74 anos, preferencialmente com mamografia digital.
- A partir dos 75 anos, o rastreamento deve ser individualizado. Recomenda-se rastreio com mamografia para mulheres que tenham expectativa de vida maior do que 7 anos, portanto uma avaliação das co-morbidades é muito importante.
Ultrassonografia
- Não existem dados que deem suporte para o rastreamento com ultrassonografia para todas as mulheres de risco populacional usual.
- Deve ser considerada como adjunto à mamografia nas mulheres com mamas densas.
- Ressonância Magnética
- Não há dados que deem suporte para o rastreamento com RM para mulheres de risco populacional usual.
Tomossíntese
- Recomenda-se que seja considerada em associação à mamografia digital, no rastreamento, quando disponível.
 RASTREAMENTO DAS MULHERES DE ALTO RISCO PARA CÂNCER DE MAMA
RASTREAMENTO DAS MULHERES DE ALTO RISCO PARA CÂNCER DE MAMA
Mamografia
- Nunca é indicado antes dos 30 anos.
- Mulheres com mutação dos genes BRCA1 ou BRCA2, ou com parentes de 1° grau com mutação provada, devem realizar o rastreamento anual com mamografia a partir dos 30 anos de idade.
- Mulheres com risco ≥ 20% ao longo da vida, calculado por um dos modelos matemáticos baseados na história familiar, devem realizar o rastreamento anual com mamografia iniciando 10 anos antes da idade do diagnóstico do parente mais jovem.
- Mulheres com história de terem sido submetidas a irradiação do tórax entre 10 e 30 anos de idade devem realizar rastreamento anual com mamografia a partir do 8° ano após o tratamento radioterápico.
- Mulheres com diagnóstico de síndromes genéticas que aumentam o risco de câncer de mama (como Li-Fraumeni, Cowden e outras) ou parentes de 1° grau acometidos devem realizar o rastreamento anual com mamografia a partir do diagnóstico.
- Mulheres com história pessoal de hiperplasia lobular atípica, carcinoma lobular in situ, hiperplasia ductal atípica, carcinoma ductal in situ e carcinoma invasor de mama devem realizar rastreamento anual com mamografia a partir do diagnóstico.
Ressonância Magnética
- Nunca é indicada antes dos 25 anos
- Mulheres com mutação dos genes BRCA1 ou BRCA2, ou com parentes de 1° grau com mutação provada, devem realizar o rastreamento anual com ressonância magnética a partir dos 25 anos de idade.
- Mulheres com risco ≥ 20% ao longo da vida, calculado por um dos modelos matemáticos baseados na história familiar, devem realizar o rastreamento anual com ressonância magnética iniciando 10 anos antes da idade do diagnóstico do parente mais jovem.
- Mulheres com história de terem sido submetidas a irradiação do tórax entre 10 e 30 anos de idade devem realizar rastreamento anual com ressonância magnética a partir do 8° ano após o tratamento radioterápico..
- Mulheres com diagnóstico de síndromes genéticas que aumentam o risco de câncer de mama (como Li-Fraumeni, Cowden e outras) ou parentes de 1° grau acometidos devem realizar o rastreamento anual com ressonância magnética a partir do diagnóstico.
- Mulheres com história pessoal de hiperplasia lobular atípica, carcinoma lobular in situ, hiperplasia ductal atípica, carcinoma ductal in situ e carcinoma invasor de mama devem realizar rastreamento anual com ressonância magnética a partir do diagnóstico.
Ultrassonografia
- Deve ser usada como substituta da ressonância magnética para mulheres que não puderem realiza-la por qualquer motivo.
Tomossíntese
- Recomenda-se que seja considerada em associação à mamografia digital no rastreamento, quando disponível.

Dra. Máryam Arbach
Grupo Intermédica - Mastologista do Hospital Renascença Campinas
Leituras recomendadas